X線レーザーで生きた細胞をナノレベルで観察することに成功
-生きた細胞を,ナノメートルの分解能で定量的に観察できる優れた手法を世界で初めて確立-
2014年1月7日
国立大学法人 北海道大学
独立行政法人理化学研究所
公益財団法人高輝度光科学研究センター
学校法人東京薬科大学
共和化工株式会社環境微生物学研究所
研究成果のポイント
• X線自由電子レーザーを用いて、生きた細胞内部のナノ構造を高コントラストで可視化。
• フェムト秒の発光時間のX線で、細胞が放射線損傷を受ける前の一瞬の姿を捉えることに成功。
• 生きた細胞内の現象の解明や、自然な状態にある生体分子のナノ構造の解明に期待。
|
北海道大学、理化学研究所(理研)、高輝度光科学研究センター(JASRI)、東京薬科大学、共和化工株式会社環境微生物学研究所は、X線自由電子レーザー(XFEL)施設SACLA※1を用いて、生きた細胞のナノレベルでの観察に成功しました。これは、北海道大学電子科学研究所の西野吉則教授、木村隆志助教、理研・放射光科学総合研究センターの別所義隆チームリーダー(現 客員研究員)、JASRIの城地保昌チームリーダーらの研究成果です。 (論文) |
背景
最先端の電子顕微鏡を用いると、物質材料を原子レベルで観察できます。しかし、どんなに優れた電子顕微鏡を用いても、生物試料に対しては、分解能がはるかに劣る観察しかできません。これは、電子線の照射により、生物試料の内部構造が壊れてしまうためです。同様に、X線顕微鏡でも、生物試料の観察では、放射線による試料損傷が分解能を制限する要因となってきました。電子顕微鏡やX線顕微鏡で用いられる線量は、放射線に耐性を持つ微生物も死んでしまうほど強力です。これらの顕微鏡では、放射線による試料損傷を軽減させるため、生物試料を極低温に保つことも行われますが、この試料処理により細胞は死んでしまうことから、生きた試料を観察することは不可能でした。
また、試料の内部構造を観察できる透過電子顕微鏡では、試料を数百ナノメートル以下の薄いスライスにしなければなりません。これは、電子線が試料を透過する能力が極めて低いためです。このため、透過電子顕微鏡では、細胞などの厚みのある試料を丸ごと観察することはできません。透過電子顕微鏡で観察できるように、細胞を固めて薄切りにすると、当然、細胞は死んでしまいます。
さらに、顕微鏡観察では、画像のコントラスト(内部構造の見やすさ)も重要な指標です。細胞などの生物試料の観察では、しばしば、試料を染色してコントラストを人為的に高めます。この方法では、染色をされた特定の構造はコントラストが強調されて見えますが、それ以外の構造を見ることは困難です。また、染色により細胞が死んでしまうこともしばしばです。
以上のように、従来の顕微鏡技術では、染色しない生きた細胞を、丸ごと、ナノメートルの分解能で観察することは不可能でした。この問題を解決するには、細胞が損傷を受ける前に、その姿を捉える手法が必要です。
XFELは、現在、日本とアメリカの2つの施設でのみ利用可能な、最先端のX線です。XFELの発光時間は10フェムト秒以下と、大型放射光施設SPring-8からのX線と比較して1,000分の1以下の短さです。フェムト秒は放射線による試料損傷が起こる時間スケールよりも短いため、XFELで試料を照らすと、試料が放射線による損傷を受ける前の一瞬の姿を捉えることができます。
しかし、先行するアメリカのXFEL施設でも、タンパク質の微小結晶やウィルス粒子など、生物試料の測定が行われてきましたが、これらの実験では、試料は真空中を飛翔しており、やはり生きた状態を保つことが困難でした。また、試料は連続的に打ち出されるため、多量の試料を用意しなければならないという問題がありました。
研究手法と成果
本研究では、Microbacterium lacticumという牛乳の中に生息する1マイクロ(100万分の1)メートル以下の大きさの微生物細胞を、生きた状態で、ナノメートルの分解能で観察しました。この微生物は、耐熱性があり、加熱殺菌時に注意が必要な厄介者です。殺菌は製品の品質保持に関わるため、この微生物の研究は、酪農においても重要性をもちますが、大きさが1マイクロメートル以下と小さいため、通常の光学顕微鏡で内部構造を観察するのが困難です。
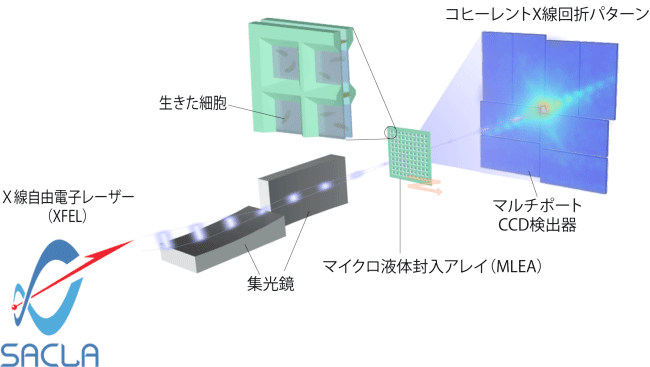
そこで本研究グループは、パルス状コヒーレントX線溶液散乱(PCXSS)法と名付けた独自に考案した手法を用いて、生きた細胞の観察に挑みました。PCXSS法の模式図を図1に示します。
PCXSS法は、自然な状態にある溶液試料を測定できるのが特徴です。これは、生物試料をマイクロ液体封入アレイ(MLEA)チップと呼ばれる、研究グループが独自に開発をしたデバイスに入れることで実現します。MLEAチップ内に封入された生物試料は、冷却、染色、切断されることなく、真空に晒されることもないため、細胞が生きている状態を保ったまま、XFELを照射できます。生物が生きていくためには水は必須であり、溶液状態で測定を行えることは、生物試料にとって、まさに理想的です。XFELは発光時間が非常に短いため、試料が放射線による損傷を受ける前に、この理想的な状態にある生物試料の姿を捉えることができます。
研究グループは、まず、MLEAチップ中で生きた細胞を閉じ込められることを、蛍光顕微鏡を使って確かめました。図2に蛍光顕微鏡観察の結果を示します。蛍光顕微鏡観察実験では、生きている細胞は緑色に、死んでいる細胞は赤色に光るように処理を施しました。図2が示すように、MLEAチップ中に細胞を封入して、1時間真空中に置いた後でも、ほとんどの細胞が生きていました。この実験により、MLEAチップを用いたPCXSS法測定によって、生きた細胞の観察が可能であることを示しました。
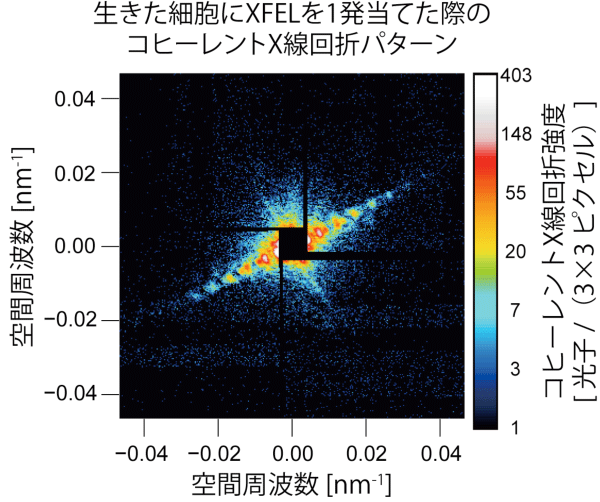
XFEL施設SACLAを用いたPCXSS法測定では、集光鏡を用いてXFELをマイクロメートル程の領域に集め、MLEAチップ中の生きた細胞に照射しました。細胞からのコヒーレントX線回折パターンを、マルチポートCCD検出器を用いて計測しました。1匹の生きた細胞に、XFELを1発照射して計測したコヒーレントX線回折パターンを図3に示します。細胞の形に由来した、綺麗な干渉縞が1方向に延びています。
PCXSS法では、対物レンズの代わりに計算機を用いて、コヒーレントX線回折パターンの測定データから、試料像を復元します。性能の良いX線用対物レンズを作ることは技術的に困難なため、対物レンズを用いないPCXSS法により、高分解能での観察が実現します。また、X線は透過性に優れ、染色をしない細胞を素通りしてしまうため、染色をしない細胞はX線にとって透明な物体です。私たちの目で透明な空気を観察するのが困難なように、通常の顕微鏡では透明な試料の観察が困難ですが、コヒーレントX線回折を用いることにより、透明な試料の内部構造も、高いコントラストで鮮明に観察できます。
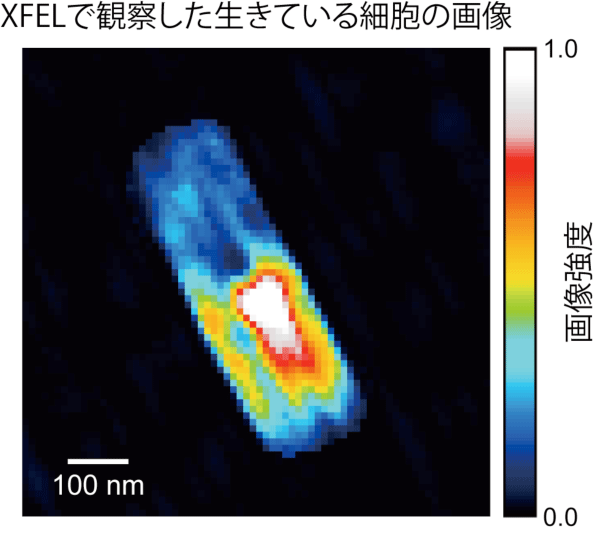
生きた細胞からのコヒーレントX線回折パターンから、計算機を用いて復元した、生きた細胞の画像を図4に示します。この細胞の画像には、極めて興味深い特徴を見ることができます。細胞の下部には、ダンベル型をした画像強度の高い部分が存在します。この領域は、X線散乱強度の強い、DNAなどの物質で構成されていることが示唆されます。実際に、細胞下部の画像強度の強い部分は核酸で構成され、それ以外の部分はタンパク質で構成されていると仮定すると、画像強度の高い部分とそれ以外の部分の強度比を、定量的にほぼ説明することができます。
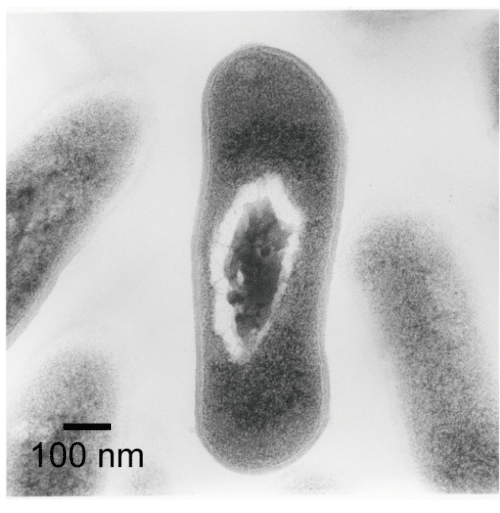
図5には、比較のため、透過電子顕微鏡で観察したMicrobacterium lacticumの画像を示します。この細胞の画像の特徴は、今回XFELを用いて観察した画像と似ています。ただし、ここで強調すべきことは、透過電子顕微鏡による測定では、細胞を樹脂で固め、100ナノメートル以下の厚さにスライスし、酢酸ウランとクエン酸鉛という重金属塩で染色するという複雑な処理をしているという点です。このような処理をした細胞の透過電子顕微鏡像を、定量的に解釈することは困難です。
今後への期待
本研究グループが世界に先駆けて開発した、XFELを用いたPCXSS法は、染色しない生きた細胞を、ナノメートルの分解能で定量的に観察できる優れた手法です。今後、生きた細胞を系統的に測定することで、未だ解明されていない原核微生物のゲノム複製やそれに続く細胞分裂などの、重要な細胞内現象の解明に繋がると期待されます。また、XFELの集光度をさらに向上させることにより、より小さな生体分子の観察や、さらなる分解能の向上も期待されます。これにより、従来の結晶構造解析などでは見ることのできなかった、自然な状態にある溶液中の生体分子のナノ構造を観察できると期待されます。生体分子のナノ構造の解明は、生命現象の理解や医学への応用へと繋がり、ライフイノベーションにも貢献します。
《参考図》
XFELを1発当てた際のコヒーレントX線回折パターン。
解析して得た、生きているMicrobacterium lacticum細胞の画像。
細胞を樹脂で固め、100ナノメートル以下の厚さにスライスし、酢酸ウランとクエン酸鉛という重金属塩で染色するという複雑な処理をしている。
《用語解説》
※1 X線自由電子レーザー(XFEL)施設SACLA
理化学研究所と高輝度光科学研究センターが共同で建設した日本で初めてのXFEL施設。第3期科学技術基本計画における5つの国家基幹技術の1つとして位置付けられ、2006年度から5年間の計画で建設・整備を進めた。2011年3月に施設が完成し、SPring-8 Angstrom Compact free electron LAserの頭文字を取ってSACLAと命名された。2011年6月に最初のX線レーザーを発振、2012年3月から共用運転が開始され、利用実験が始まっている。
※2 フェムト秒
1,000兆分の1秒が1フェムト秒。1フェムト秒は、光の速さ(秒速約30万キロメートル)でも0.3マイクロメートルしか進むことができないほどの極めて短い時間。
※3 コヒーレントX線回折
波面が揃っている光のことをコヒーレントな光といい、レーザー光の持つ特徴の1つ。コヒーレントなX線を試料に照射した際に起こるX線の散乱現象が、コヒーレントX線回折である。コヒーレントX線回折パターンは、試料の僅かな構造の違いにも敏感である。コヒーレントX線回折パターンを計算機で解析すると、試料の画像を得ることができる。
|
《問い合わせ先》 (SPring-8に関すること) |
《問い合わせ先》
北海道大学電子科学研究所
教授 西野 吉則(にしの よしのり)
TEL:011-706-9354 FAX:011-706-9355
E-mail:yoshinori.nishino[at]hokudai.ac.jp
ホームページ:http://cxo-www.es.hokudai.ac.jp/
(SPring-8に関すること)
公益財団法人 高輝度光科学研究センター 広報室
TEL:0791-58-2785 FAX:0791-58-2786
E-mail:このメールアドレスはスパムボットから保護されています。閲覧するにはJavaScriptを有効にする必要があります。